Des techniques synchrotrons révèlent l’action d’une molécule métallo-organique dans des cellules d’une forme agressive du cancer du sein

Le cancer du sein type triple négatif (TNBC en anglais, "triple negative breast cancer"), représente 10 à 20% des cas de cancers du sein. Il se caractérise par l’absence de récepteur des œstrogènes, de récepteur de la progestérone et de récepteurs du facteur de croissance épidermique humaine (HER2). Ceci signifie qu'il ne répond ni à l’hormonothérapie ni à l’immunothérapie. Le manque de cibles moléculaires pour le traitement adapté de ce type de cancer très agressif reste un défi pour la communauté scientifique et médicale.
Une équipe pluridisciplinaire de l'Institut national de la santé et de la recherche médicale (Inserm), du CNRS, de Sorbonne université, de l'université PSL, de l'Université Grenoble Alpes et de l'ESRF, a étudié une molécule organométallique de la famille des métallocènes, un dérivé du métabolite actif du tamoxifène, - un médicament oral d'hormonothérapie très utilisé pour la prévention et le traitement du cancer du sein non invasif et invasif-, et précisé son mécanisme d’action au sein de cellules de cancer du sein type triple négatif.
Ces composés organométalliques ont été développés par le professeur G. Jaouen et son groupe à Sorbonne université et à l'université PSL à Paris. Ils ont démontré leur large spectre d'efficacité envers différents types de cellules cancéreuses et leur potentiel à surmonter la résistance aux médicaments anticancéreux.
"Nous connaissions l’efficacité de cette molécule à base d’osmium grâce aux travaux approfondis déjà effectués. Mais, nous ne connaissions pas exactement son mécanisme d’action dans des cellules de cancer du sein type triple-négatif. C'est pourquoi nous avons localisé et mesuré les concentrations de cette molécule à l'intérieur même de la cellule cancéreuse, afin de mieux évaluer son efficacité", explique Sylvain Bohic, chercheur Inserm et auteur principal de l'étude.
Les chercheurs ont utilisé la ligne de lumière ID16A pour leur expérience. La technique de pointe de nano-imagerie synchrotron permet un éclairage unique sur la distribution intracellulaire de ce métallocène, avec une résolution de 35 nanomètres. "Depuis plusieurs années, les recherches sont menées dans ce domaine. Aujourd’hui, elles bénéficient des dernières techniques en matière de cryo-fluorescence des rayons X en 2D et 3D" explique Peter Cloetens, scientifique ESRF, en charge de ID16A.
Pour la première fois, l’équipe scientifique a montré comment la molécule pénètre aisément les membranes de la cellule cancéreuse en raison de sa nature lipophile et comment elle cible un organite cellulaire essentiel, le réticulum endoplasmique, un réseau de tubules membranaires (souvent interconnectées) dispersées dans tout le cytoplasme des cellules eucaryotes. La molécule, un dérivé osmocénique de l’hydroxytamoxifène, qui est oxydée à cet endroit engendre des métabolites qui vont attaquer différentes parties de la cellule en même temps, menant à l'activité anticancéreuse observée. "la cellule cancéreuse doit faire face à de nombreux feux démarrant à différents endroits dans la cellule. La cellule tumorale, débordée par autant d’attaques, ne peut faire face et meurt, ou s’inactive", explique Sylvain Bohic.
Les résultats sont prometteurs. En effet, cette nouvelle famille de composés organométalliques, qui présentent un mécanisme d'action multi-cibles, pourrait devenir une alternative intéressante dans l’arsenal de chimiothérapie classique et, permettre de surmonter la résistance aux médicaments actuels tout en ayant un coût faible. Le médicament Cisplatine, une autre molécule contenant un métal de transition qui est largement utilisé pour le traitement du cancer, a comme cible primaire l'ADN qu’il endommage à l'intérieur de la cellule. Souvent efficace, il a cependant des effets secondaires et les cellules cancéreuses développent aussi des mécanismes de résistance à ce type de chimiothérapie. Le cancer du sein triple négatif, comme d’autres cancers, est souvent résistant au Cisplatine. "Cette étude contribue au développement de mécanismes alternatifs à ceux des molécules de chimiothérapie classique utilisées dans le traitement des cancers. Nous sommes au début de cette recherche. A ce stade, des tests cliniques ne peuvent être envisagés, mais cette étude est prometteuse", indique le professeur Jaouen co-auteur de cette étude.
La prochaine étape est de découvrir comment cette molécule agit sur des cellules saines et d'étudier sa toxicologie.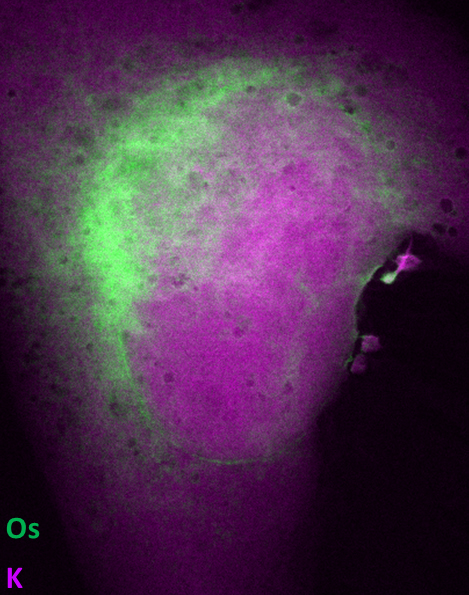
Mis à jour le 15 décembre 2019
Référence
Florin Fus, Yang Yang, Shirley Lee, Siden Top, Marie Carrière, Alexandre Bouron, Alexandra Pacureanu, Julio Da silva, Michèle Salmain, Anne Vessières, Peter Cloetens, Gérard Jaouen, Sylvain Bohic.
Angewandte Chemie, janvier 2019
DOI : 10.1002/anie.201812336

